

醫(yī)療器械生產(chǎn)企業(yè)合規(guī)技術(shù)咨詢服務(wù)
注冊備案 · 臨床試驗(yàn) · 體系建立輔導(dǎo) · 分類界定 · 申請創(chuàng)新
186-0382-3910

第三類體外診斷試劑注冊證變更(登記事項(xiàng)變更)服務(wù)
依據(jù)《體外診斷試劑注冊管理辦法》相關(guān)規(guī)定,第三類體外診斷試劑實(shí)行注冊管理。已注冊的第三類體外診斷試劑,醫(yī)療器械注冊證及其附件載明的內(nèi)容發(fā)生變化,注冊人應(yīng)當(dāng)向原注冊...
服務(wù)價(jià):¥電議
好評系數(shù):

依據(jù)《體外診斷試劑注冊管理辦法》相關(guān)規(guī)定,第三類體外診斷試劑實(shí)行注冊管理。已注冊的第三類體外診斷試劑,醫(yī)療器械注冊證及其附件載明的內(nèi)容發(fā)生變化,注冊人應(yīng)當(dāng)向原注冊部門申請注冊變更,并按照相關(guān)要求提交申報(bào)資料。登記事項(xiàng)變更資料符合要求的,食品藥品監(jiān)督管理部門應(yīng)當(dāng)在10個(gè)工作日內(nèi)發(fā)給醫(yī)療器械注冊變更文件。登記事項(xiàng)變更資料不齊全或者不符合形式審查要求的,食品藥品監(jiān)督管理部門應(yīng)當(dāng)一次告知需要補(bǔ)正的全部內(nèi)容。
未依法辦理注冊登記事項(xiàng)變更有何后果
未依法辦理第三類體外診斷試劑注冊登記事項(xiàng)變更的,由縣級以上人民政府食品藥品監(jiān)督管理部門責(zé)令限期改正;逾期不改正的,向社會(huì)公告未備案單位和產(chǎn)品名稱,可以處1萬元以下罰款。其次,應(yīng)該提早辦理變更登記,以防臨檢仍處于辦理階段出現(xiàn)。
有以下情形的,需辦理注冊證登記事項(xiàng)變更
1、注冊人名稱變更、注冊人住所變更;
2、境內(nèi)體外診斷試劑生產(chǎn)地址變更;
3、代理人變更、代理人住所變更。
注意:注冊人應(yīng)在相應(yīng)的生產(chǎn)許可變更后辦理登記事項(xiàng)變更。
辦理三類IVD注冊證(登記事項(xiàng)變更)所需材料
1、申請表;
2、證明性文件:營業(yè)執(zhí)照和組織機(jī)構(gòu)代碼證;
3、注冊人關(guān)于變更情況的聲明;
4、原醫(yī)療器械注冊證及其附件的復(fù)印件、歷次醫(yī)療器械注冊變更文件復(fù)印件;
5、關(guān)于變更情況相關(guān)的申報(bào)資料要求:企業(yè)名稱變更核準(zhǔn)通知書、相應(yīng)詳細(xì)變更情況說明及相應(yīng)證明文件、應(yīng)當(dāng)提供相應(yīng)變更后的生產(chǎn)許可證。
第三類IVD注冊變更(登記事項(xiàng)變更)服務(wù)流程
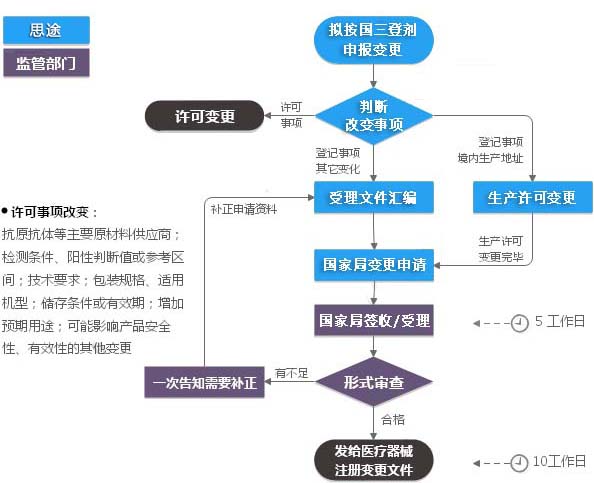
第三類IVD注冊變更(登記事項(xiàng)變更)官方收費(fèi)標(biāo)準(zhǔn)
辦理三類IVD注冊證登記事項(xiàng)變更,官方不收取變更申請費(fèi)用。
第三類IVD注冊變更(登記事項(xiàng)變更)服務(wù)辦理依據(jù)
| 文件名稱 | 文號 |
|---|---|
| 《醫(yī)療器械監(jiān)督管理?xiàng)l例》 | 650號文件 |
| 《體外診斷試劑注冊管理辦法》 | 局令5號 |
| 關(guān)于公布體外診斷試劑注冊申報(bào)資料要求和批準(zhǔn)證明文件格式的公告 | 2014年44號 |
第三類IVD注冊變更(登記事項(xiàng)變更)服務(wù)周期
立項(xiàng)階段
預(yù)算、合同、考慮期,7個(gè)工作日。
受理前資料準(zhǔn)備
資料收集、申報(bào)資料撰寫、資料確認(rèn)、蓋章,預(yù)計(jì)15個(gè)工作日。
申請后
登記事項(xiàng)變更法規(guī)時(shí)間15個(gè)工作日,約1個(gè)月。
預(yù)算合計(jì)
立項(xiàng)后至注冊登記變更完成,約2個(gè)月。
第三類IVD注冊變更(登記事項(xiàng)變更)推薦服務(wù)
| 三類IVD產(chǎn)品注冊服務(wù) | 二類IVD產(chǎn)品注冊服務(wù) |
| IVD臨床試驗(yàn)服務(wù) | GMP年度輔導(dǎo)服務(wù) |

立即咨詢
 最新文章
最新文章 2025-08-31
2025-08-31 2025-08-31
2025-08-31 2025-08-31
2025-08-31 2025-08-31
2025-08-31 2025-08-31
2025-08-31 精選案例
精選案例
遠(yuǎn)紅外穴位貼/前列腺遠(yuǎn)紅外穴位貼臨床試驗(yàn)注冊案例
醫(yī)用疤痕/遠(yuǎn)紅外治療凝膠臨床試驗(yàn)注冊案例
脈沖磁場穴位治療儀同品種比對產(chǎn)品注冊案例

生物玻璃創(chuàng)面無機(jī)敷料醫(yī)療器械產(chǎn)品注冊證申辦案例

牙齒脫敏劑醫(yī)療器械注冊免臨床GMP案例

醫(yī)用冷凍箱醫(yī)療器械注冊免臨床體系建立案例

醫(yī)用冷藏箱醫(yī)療器械注冊GMP體系認(rèn)證案例
定制式活動(dòng)義齒醫(yī)療器械注冊證變更案例
醫(yī)用紅外額溫計(jì)(額溫槍)臨床驗(yàn)證注冊案例
下肢運(yùn)動(dòng)康復(fù)訓(xùn)練機(jī)產(chǎn)品注冊體系案例
八年
醫(yī)療器械服務(wù)經(jīng)驗(yàn)
-
多一份參考,總有益處
聯(lián)系思途,免費(fèi)獲得專屬《落地解決方案》及報(bào)價(jià)
咨詢相關(guān)問題或咨詢報(bào)價(jià),可以直接與我們聯(lián)系
思途CRO——醫(yī)療器械注冊臨床第三方平臺(tái)
- 在線咨詢
- 在線客服
- 服務(wù)熱線
北京公司
186-0382-3911鄭州公司
186-0382-3910合肥公司
188-5696-0331 - 微信咨詢

- 返回頂部


 豫公網(wǎng)安備 41010202003160號
豫公網(wǎng)安備 41010202003160號