醫(yī)療器械注冊單元劃分概述——注冊單元劃分常見問題解答
從事醫(yī)療器械注冊的小伙伴們可能都為同一個問題苦惱過,那就是醫(yī)療器械注冊單元的劃分。企業(yè)所設(shè)計開發(fā)出的產(chǎn)品,其所包含的產(chǎn)品范圍,是否可通過一個注冊單元完成注冊,從而


注冊備案 · 臨床試驗 · 體系建立輔導(dǎo) · 分類界定 · 申請創(chuàng)新
來源:醫(yī)療器械注冊代辦 發(fā)布日期:2024-06-27 閱讀量:次
在醫(yī)療健康行業(yè)中,醫(yī)療器械作為疾病診斷、治療、預(yù)防和監(jiān)護(hù)的重要工具,其安全性和有效性是保障公眾健康的基礎(chǔ)。我國對醫(yī)療器械實施分類管理,根據(jù)風(fēng)險程度將其分為第一類、第二類和第三類,其中二類醫(yī)療器械屬于中等風(fēng)險級別,如X光機(jī)、超聲波診斷設(shè)備等。為了確保這些產(chǎn)品符合國家規(guī)定的安全和質(zhì)量標(biāo)準(zhǔn),其上市前必須通過國家藥品監(jiān)督管理局(NMPA)的注冊審批。本文將詳細(xì)解析二類醫(yī)療器械注冊證的費用構(gòu)成,為企業(yè)提供實用的指南。
醫(yī)療器械注冊費用并非單一項目,而是由多個環(huán)節(jié)產(chǎn)生的費用綜合而成。通常,這些費用包括但不限于產(chǎn)品檢測費、臨床試驗費(如適用)、質(zhì)量管理體系(GMP)認(rèn)證費、注冊申報費等。根據(jù)產(chǎn)品特性和注冊過程的復(fù)雜程度,總費用可從數(shù)萬元至數(shù)十萬元不等。
1、產(chǎn)品檢測費用:這是注冊前的必備環(huán)節(jié),需由有資質(zhì)的第三方CMA檢測機(jī)構(gòu)進(jìn)行(通常選擇藥監(jiān)下屬的檢測所,周期較慢),費用依產(chǎn)品類型和檢測項目而定,大約在幾千至1萬元之間。
2、臨床試驗費用:對于某些需要通過臨床試驗來證明其安全性和有效性的二類醫(yī)療器械,臨床試驗成為費用的大頭,成本從幾萬到十幾萬元不等,具體取決于產(chǎn)品的復(fù)雜度,具體費用需要臨床部門細(xì)算。然而,若能通過同品種比對等途徑避免臨床試驗,這一部分費用可以完全節(jié)省。
3、GMP認(rèn)證費用:確保醫(yī)療器械的生產(chǎn)過程符合良好生產(chǎn)規(guī)范(GMP)標(biāo)準(zhǔn),這一環(huán)節(jié)正常來說是免費的,但有可能會卡你,多多少少都能抓點問題出來。
4、注冊申報費用:包括各省藥品監(jiān)督管理部門收取的固定行政性收費,一般從免費至數(shù)萬元不等。具體可查看生產(chǎn)企業(yè)所在省份藥監(jiān)局的收費標(biāo)準(zhǔn)。
總的來說,二類醫(yī)療器械注冊證的獲取是一個復(fù)雜且成本不菲的過程,費用從幾萬到二十萬不等。企業(yè)需要對各個環(huán)節(jié)有清晰的認(rèn)識和周密的準(zhǔn)備,通過科學(xué)規(guī)劃、合理選擇注冊策略,并充分利用現(xiàn)有資源,可以在確保產(chǎn)品質(zhì)量的同時,有效控制成本,加速產(chǎn)品上市進(jìn)程。當(dāng)然,選擇將二類醫(yī)療器械注冊全流程外包,也是個不錯的選擇。

站點聲明
本網(wǎng)站所提供的信息僅供參考之用,并不代表本網(wǎng)贊同其觀點,也不代表本網(wǎng)對其真實性負(fù)責(zé)。圖片版權(quán)歸原作者所有,如有侵權(quán)請聯(lián)系我們,我們立刻刪除。如有關(guān)于作品內(nèi)容、版權(quán)或其它問題請于作品發(fā)表后的30日內(nèi)與本站聯(lián)系,本網(wǎng)將迅速給您回應(yīng)并做相關(guān)處理。
鄭州思途醫(yī)療科技有限公司專注于醫(yī)療器械產(chǎn)品政策與法規(guī)規(guī)事務(wù)服務(wù),提供產(chǎn)品注冊備案申報代理、臨床試驗、體系建立輔導(dǎo)、分類界定、申請創(chuàng)新辦理服務(wù)。

從事醫(yī)療器械注冊的小伙伴們可能都為同一個問題苦惱過,那就是醫(yī)療器械注冊單元的劃分。企業(yè)所設(shè)計開發(fā)出的產(chǎn)品,其所包含的產(chǎn)品范圍,是否可通過一個注冊單元完成注冊,從而
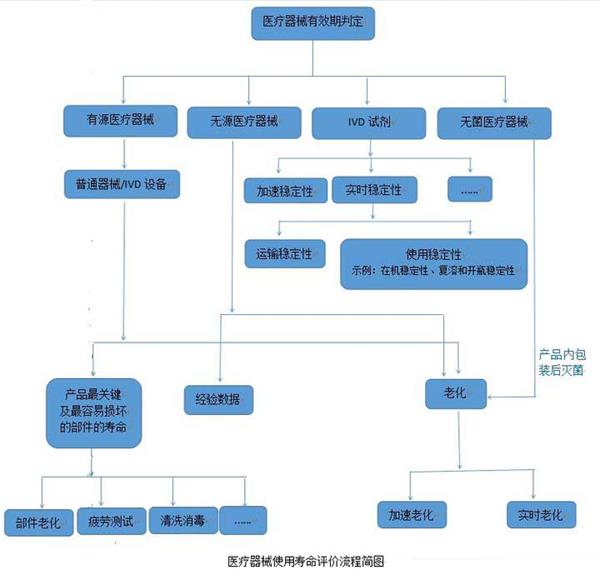
醫(yī)療器械的使用壽命是指醫(yī)療器械從規(guī)劃、設(shè)計、生產(chǎn)、銷售、安裝調(diào)試到使用、維修、維護(hù)檢測、報廢的全過程。而醫(yī)院使用的醫(yī)療器械的應(yīng)用質(zhì)量和安全管理在整個壽命過程中占重

隨著醫(yī)療器械出口的日益增長,根據(jù)市場的需求各醫(yī)療器械生產(chǎn)廠商需要符合國家和地區(qū)的質(zhì)量體系法規(guī)越來越多,所以經(jīng)常會碰到出處于不同法規(guī)或標(biāo)準(zhǔn)的一些比較容易混淆的概念及

剛接觸醫(yī)療器械CRO行業(yè)的小伙伴,在學(xué)習(xí)文件法規(guī)資料的同時,常看到一些英文類專業(yè)名詞不知道是什么意思。下面,一起看看常見的醫(yī)療器械臨床試驗專業(yè)術(shù)語......"

2019年5月31日,國家藥監(jiān)局發(fā)布了《關(guān)于實施醫(yī)療器械注冊電子申報的公告(2019年第46號)》,從2019年6月24日正式實施電子申報,從11月1日起提交國家局的注冊資料都需要按照電子申報目錄

醫(yī)療器械注冊證是依照法定程序,對擬上市銷售、使用的醫(yī)療器械的安全性、有效性進(jìn)行評價,決定同意其銷售、使用后發(fā)放的證件,由國家食品藥品監(jiān)督管理總局統(tǒng)一制定。"

化妝品分為國產(chǎn)和進(jìn)口、又分為非特殊化妝品和特殊化妝品,備案的費用和周期各不相同,具體各類化妝品備案多少錢?周期要多久?看完就懂了......
眾所周知,醫(yī)療器械分為三類,一類采用備案制,二三類采用注冊制管理,等級越高,管理越嚴(yán)格。一類醫(yī)療器械都是免臨床的,因此備案工作比較簡單不繁瑣。而二三類醫(yī)療器械除免臨床產(chǎn)品
臨床試驗得出正確的結(jié)論需要嚴(yán)謹(jǐn)?shù)脑囼炘O(shè)計,雙盲隨機(jī)平行對照臨床試驗仍是證據(jù)等級最高的原始研究。根據(jù)《醫(yī)療器械臨床試驗設(shè)計指導(dǎo)原則》(2018年第6號)(下稱《原則》),隨

根據(jù)《醫(yī)療器械監(jiān)督管理條例》(國務(wù)院令第650號),第三類醫(yī)療器械注冊時需要提交產(chǎn)品的檢測報告,并且注冊申請資料中的產(chǎn)品檢測報告應(yīng)當(dāng)由具有承檢資格的醫(yī)療器械檢驗機(jī)構(gòu)出具
行業(yè)資訊
?
?
?
?
?
?
知識分享
法規(guī)文件
?
?
?
?
?
?
八年
醫(yī)療器械服務(wù)經(jīng)驗
聯(lián)系思途,免費獲得專屬《落地解決方案》及報價
咨詢相關(guān)問題或咨詢報價,可以直接與我們聯(lián)系
思途CRO——醫(yī)療器械注冊臨床第三方平臺
