國內凝血分析流水線產品盤點(沃芬/希森美康/思塔高和艾科達)
隨著國家醫(yī)療改革的不斷深入,使得綜合性大中型醫(yī)療機構的中心實驗室對自動化系統(tǒng)有了新的要求,為了簡化檢測流程,提高檢測效率,保證數據準確度等,中心實驗室對集中化診斷


注冊備案 · 臨床試驗 · 體系建立輔導 · 分類界定 · 申請創(chuàng)新
來源:醫(yī)療器械注冊代辦 發(fā)布日期:2022-07-06 閱讀量:次
前段時間一個朋友發(fā)了一個截圖給我,說他檢索到美國有2萬多名CRA,問我:“你們知道的數據比較多,國內目前到底有多少CRA啊?”
圖:公開資料顯示美國有22574名CRA,71.7%為女性,28.%為男性,平均年齡為44歲
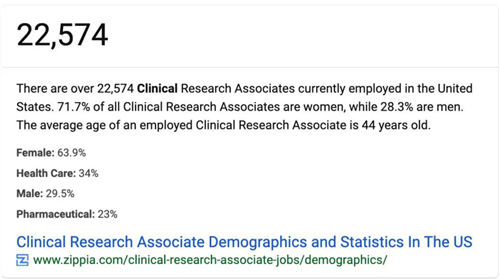
計算國內CRA數量的方法可能有很多種,如下兩種個人覺得還是相對靠譜的:
方法一:統(tǒng)計行業(yè)內各家CRO、藥企公司內CRA數量,相加即可。
方法二:通過分析在研臨床試驗以及覆蓋的中心數量,然后根據行業(yè)平均每個CRA負責中心數,最后利用行業(yè)在研中心數除以單個CRA平均負責中心數,即可得到CRA數量。
當然方法一肯定更加精準,但執(zhí)行起來難度比較大,基于數據優(yōu)勢,今天用方法二給大家大致推算國內到底有多少CRA!
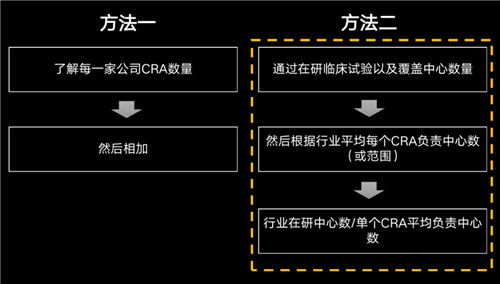
利用使用方法二計算國內CRA數量,首先要了解國內在研的臨床研究及覆蓋中心情況!
我們對CDE藥物臨床試驗信息登記與公示平臺的試驗做了分析,截至2022年5月28日,在CDE登記公示平臺上標識為“進行中”的項目有7713個,當然“進行中”也包含3種狀態(tài),分別是“尚未招募”、“招募中”及“招募完成”。
如果已經在CDE平臺登記且狀態(tài)是“進行中-尚未招募”大概率項目還在SSU期間,這類項目有2625個;
“進行中-招募中”項目有3510個,這類項目大家可以當做是在入組期!
“進行中-招募完成”項目有1575個,這類項目應該在隨訪或關中心期!

7713個“在研”項目分布在1520家中心,1520是去重之后的結果,如果不去重,則有78020個Site頻次有在研的項目在進行!
我們知道在CDE登記的都是注冊類藥物試驗,針對注冊類項目,有過CRA相關經驗的都知道,每個CRA負責中心數一般在2~8家。
當然CRA負責的中心數量和CRA經驗、企業(yè)性質(CRO or 藥企)、項目類型、項目階段、入組受試者數量等很多因素有關系。
今天我們用平均數5作為行業(yè)的“單個CRA平均負責中心數”。大家不用太較真這個數字是不是精準,因為今天只是介紹一種方法,得出一個相對靠譜的、可供大家參考的粗略數字。
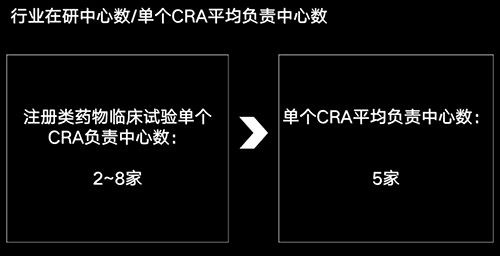
這樣國內CRA數量就呼之欲出了,78020 ? 5= 15604。當然這是基于CDE公示的臨床試驗數算出來的,而大家都知道,在CDE登記公示的臨床試驗都是注冊類藥物臨床試驗,所以可以得出這樣的結論:國內從事注冊類藥物臨床試驗監(jiān)查的CRA差不多有1.5萬人!
除了注冊類藥物臨床試驗,我們知道還有大量的CRA在負責上市后的藥物臨床試驗,另外也有不少器械類的CRA!

當然在“中國臨床試驗注冊中心”上登記了很多非注冊類藥物及一些器械類試驗,因為絕大部分都是IIT(研究者發(fā)起類)研究,這些項目很多不一定有監(jiān)查,所以不太能作為參考數據!
不過個人經驗,綜合以上3個部分,國內CRA數量和美國應該差別不大,往多一點說應該在3萬左右!
之前聽行業(yè)內有人說5萬、甚至10萬的,肯定是達不到的!
注:有的朋友可能會提醒,在CDE登記公示的試驗可能不夠精準,確實有一些企業(yè)會晚一些更新自己的試驗狀態(tài),有可能試驗結束了顯示的還是“進行中”,甚至新增或刪除了一些中心也沒有及時上去更新。這一點大家不用太擔心,這幾年隨著CDE及藥物臨床試驗機構對這塊試驗公開的信息重視,信息登記公示越來越精準,這個原因造成的誤差沒有這么大!

站點聲明
本網站所提供的信息僅供參考之用,并不代表本網贊同其觀點,也不代表本網對其真實性負責。圖片版權歸原作者所有,如有侵權請聯系我們,我們立刻刪除。如有關于作品內容、版權或其它問題請于作品發(fā)表后的30日內與本站聯系,本網將迅速給您回應并做相關處理。
鄭州思途醫(yī)療科技有限公司專注于醫(yī)療器械產品政策與法規(guī)規(guī)事務服務,提供產品注冊備案申報代理、臨床試驗、體系建立輔導、分類界定、申請創(chuàng)新辦理服務。

隨著國家醫(yī)療改革的不斷深入,使得綜合性大中型醫(yī)療機構的中心實驗室對自動化系統(tǒng)有了新的要求,為了簡化檢測流程,提高檢測效率,保證數據準確度等,中心實驗室對集中化診斷

盡管處在一個快速發(fā)展的陽光產業(yè),在機會面前中國CRC也面臨著很多挑戰(zhàn),這些挑戰(zhàn)大致可以包括:工作強度大、任務重、壓力大;協調工作難度大,不可控因素多;工作繁雜,工作交

近日美國食品藥品監(jiān)督管理局(FDA)更新了《醫(yī)療器械提交的反饋申請和會議申請:Q-Submission指導原則》。此文件是對2019版Q-sub指導原則的更新,更新的主要內容如下:1. 增加了STeP醫(yī)療

一個產品帶有CE 標志(標記) 也就意味著其制造商宣告:該產品符合歐洲的健康、安全、與環(huán)境保護之相關法律中所規(guī)定 的基本要求。因而該產品是對:使用者(譯者注:人)、寵物(
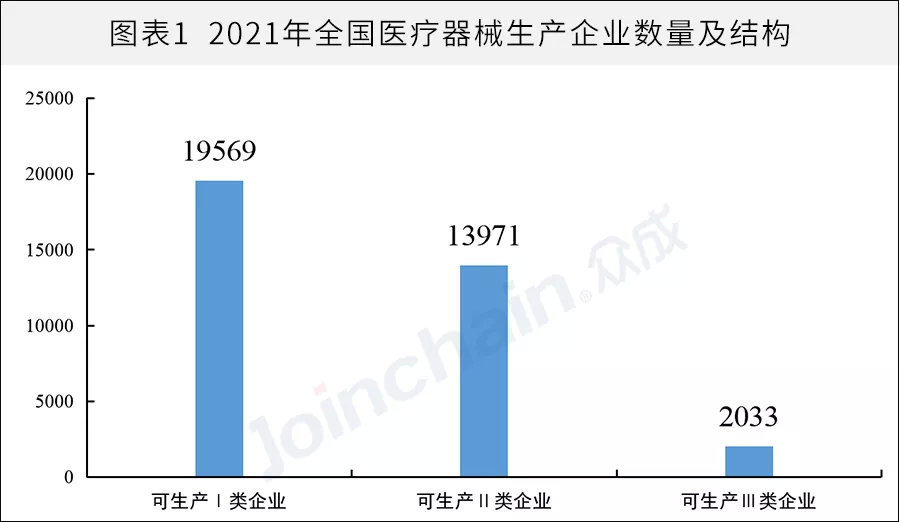
據眾成數科統(tǒng)計,截至2021年12月31日,全國醫(yī)療器械生產企業(yè)數量達28954家,較2020年的25440家同比增長13.8%。其中,可生產Ⅰ類產品企業(yè)19569家,可生產Ⅱ類產品13971家,可生產Ⅲ類產品
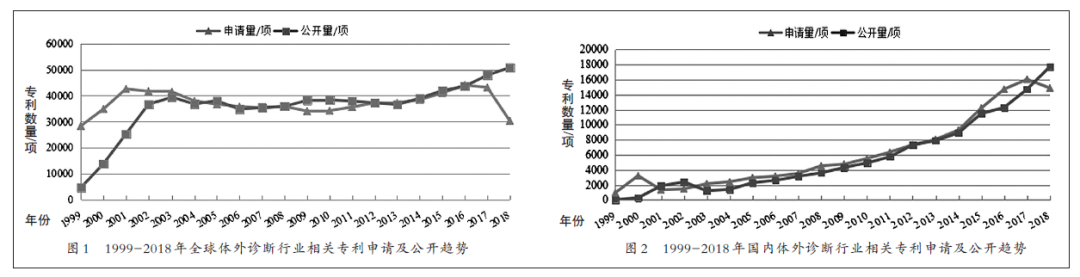
體外診斷(In Vitro Diagnosis,下稱IVD),是在人體之外,通過對人體樣本(血液、體液、組織等)進行檢測而獲取臨床診斷信息,進而判斷疾病或機體功能的產品和服務。IVD已經成為人類

藥品/化妝品/醫(yī)療器械企業(yè)賣假貨無證銷售罰多少錢?近期福建省發(fā)布藥品醫(yī)療器械化妝品賣假貨無證銷售典型案例,一起來看看懲罰力度和罰款額度。"

美國食品藥品監(jiān)督管理局FDA宣布,其計劃采用ISO13485標準作為其質量體系立法的基礎。FDA如采用ISO13485標準替代其現有的質量體系法規(guī),則代表該標準的認可度獲得進一步的提高,已經成

在鶴壁辦理一張醫(yī)療器械經營許可證要多少錢?只要有人員有場地滿足辦理的要求,就可以自行辦理。自行辦理是免費的哦!本文為大家科普一下找代辦機構辦理的情況下,鶴壁醫(yī)療器械經營許

隨著醫(yī)療水平的不斷提高,醫(yī)療器械已被廣泛用于疾病診斷、預防、監(jiān)護、治療和康復等領域。任何已批準上市的醫(yī)療器械都不是絕對安全的,只有通過持續(xù)開展醫(yī)療器械不良事件監(jiān)測
行業(yè)資訊
知識分享
八年
醫(yī)療器械服務經驗
聯系思途,免費獲得專屬《落地解決方案》及報價
咨詢相關問題或咨詢報價,可以直接與我們聯系
思途CRO——醫(yī)療器械注冊臨床第三方平臺
