【國(guó)家化妝品備案查詢(xún)】國(guó)家化妝品備案查詢(xún)網(wǎng)站入口
2020年8月14日,化妝品備案網(wǎng)系統(tǒng)和檢測(cè)系統(tǒng)更新了!國(guó)家化妝品備案查詢(xún)需要移步到新網(wǎng)址了!


注冊(cè)備案 · 臨床試驗(yàn) · 體系建立輔導(dǎo) · 分類(lèi)界定 · 申請(qǐng)創(chuàng)新
來(lái)源:醫(yī)療器械注冊(cè)代辦 發(fā)布日期:2021-03-14 閱讀量:次
消字號(hào)是我國(guó)衛(wèi)生消毒用品的專(zhuān)用批準(zhǔn)文號(hào),屬于衛(wèi)生行政部門(mén)管理的非藥品類(lèi)產(chǎn)品,主要包括消毒劑、消毒器械和衛(wèi)生用品三大類(lèi)。這類(lèi)產(chǎn)品僅具備消毒、抑菌或殺菌功能,不能宣稱(chēng)任何治療效果,其檢測(cè)指標(biāo)需符合《消毒技術(shù)規(guī)范》等國(guó)家標(biāo)準(zhǔn)。例如,常見(jiàn)的84消毒液、紫外線消毒燈、女性抗菌洗液等均屬于消字號(hào)范疇。與藥品(國(guó)藥準(zhǔn)字號(hào))不同,消字號(hào)產(chǎn)品由省級(jí)以下衛(wèi)生行政部門(mén)審批,申報(bào)周期短、費(fèi)用低,但需嚴(yán)格遵循備案管理要求。

申請(qǐng)主體限制:個(gè)體工商戶或個(gè)人不得申請(qǐng)消字號(hào)備案,必須是具備獨(dú)立法人資格的企業(yè)或工廠,例如生物科技公司、制藥企業(yè)等。
生產(chǎn)資質(zhì)要求:若企業(yè)自主生產(chǎn),需取得《消毒產(chǎn)品生產(chǎn)企業(yè)衛(wèi)生許可證》;若委托生產(chǎn),需與受托方簽訂合同并提供其生產(chǎn)資質(zhì)證明。
人員與設(shè)施:企業(yè)需配備專(zhuān)業(yè)衛(wèi)生管理人員,生產(chǎn)場(chǎng)地布局、工藝流程需符合《消毒產(chǎn)品生產(chǎn)企業(yè)衛(wèi)生規(guī)范》,從業(yè)人員需通過(guò)健康檢查與衛(wèi)生知識(shí)培訓(xùn)。
禁用成分:配方中嚴(yán)禁添加抗生素、抗真菌藥物、激素等處方藥成分,以及衛(wèi)生行政部門(mén)公布的禁用物質(zhì)(如部分化學(xué)防腐劑)。原料需符合《中國(guó)藥典》《化妝品安全技術(shù)規(guī)范》等標(biāo)準(zhǔn),例如酒精濃度、植物提取物純度等。
配方審核重點(diǎn):消毒劑需明確有效成分含量及作用機(jī)理;抗(抑)菌洗劑需提交完整配方;消毒器械需提供結(jié)構(gòu)圖或元器件清單。若涉及食品相關(guān)用途(如餐具消毒劑),還需額外檢測(cè)鉛、砷等重金屬殘留。
消字號(hào)產(chǎn)品按風(fēng)險(xiǎn)等級(jí)分為三類(lèi),備案要求差異顯著:
1. 消毒劑與消毒器械:
- 第一類(lèi)(高風(fēng)險(xiǎn)):包括用于醫(yī)療器械滅菌、皮膚黏膜消毒的產(chǎn)品,需提交衛(wèi)生安全評(píng)價(jià)報(bào)告(含理化指標(biāo)、微生物殺滅試驗(yàn)、毒理試驗(yàn)等),并向省級(jí)衛(wèi)生部門(mén)備案。
- 第二類(lèi)(中風(fēng)險(xiǎn)):如環(huán)境消毒劑,備案時(shí)需檢測(cè)有效成分含量、pH值、穩(wěn)定性及殺菌效果。
2. 衛(wèi)生用品:如濕巾、抗抑菌凝膠等,備案材料包括產(chǎn)品標(biāo)簽樣稿、檢驗(yàn)報(bào)告、生產(chǎn)許可證復(fù)印件等,檢測(cè)項(xiàng)目涵蓋微生物指標(biāo)、刺激性試驗(yàn)等。
檢測(cè)機(jī)構(gòu)資質(zhì):檢測(cè)須由CMA(中國(guó)計(jì)量認(rèn)證)或CNAS(中國(guó)合格評(píng)定國(guó)家認(rèn)可委員會(huì))認(rèn)可的第三方實(shí)驗(yàn)室完成。
核心材料清單:
- 產(chǎn)品配方或器械結(jié)構(gòu)圖
- 生產(chǎn)工藝流程圖
- 檢驗(yàn)報(bào)告(需加蓋檢測(cè)機(jī)構(gòu)騎縫章)
- 標(biāo)簽及說(shuō)明書(shū)樣稿(禁止標(biāo)注“治療”“消炎”等違規(guī)宣稱(chēng))
- 企業(yè)營(yíng)業(yè)執(zhí)照與生產(chǎn)許可證
- 衛(wèi)生安全責(zé)任保證書(shū)
備案流程:
1. 材料準(zhǔn)備:明確產(chǎn)品類(lèi)別與檢測(cè)項(xiàng)目,起草企業(yè)標(biāo)準(zhǔn)或質(zhì)量標(biāo)準(zhǔn)。
2. 樣品送檢:同一批次樣品需完成所有檢測(cè)項(xiàng)目,如消毒劑需進(jìn)行加速穩(wěn)定性試驗(yàn)(37℃保存90天)。
3. 網(wǎng)上申報(bào):通過(guò)省級(jí)衛(wèi)生健康委員會(huì)備案系統(tǒng)提交材料,涉密資料可線下補(bǔ)充。
4. 形式審查:衛(wèi)生部門(mén)在5個(gè)工作日內(nèi)完成審核,通過(guò)后發(fā)放備案憑證。
備案延續(xù)要求:第一類(lèi)產(chǎn)品衛(wèi)生安全評(píng)價(jià)報(bào)告有效期為4年,到期前需重新檢測(cè)并提交材料;第二類(lèi)產(chǎn)品報(bào)告長(zhǎng)期有效,但若配方、工藝變更需重新備案。
1. 宣傳合規(guī):產(chǎn)品包裝及廣告中不得出現(xiàn)“治療”“藥用”等誤導(dǎo)性詞匯,僅可標(biāo)注“抑菌率≥90%”等實(shí)測(cè)數(shù)據(jù)。
2. 標(biāo)簽規(guī)范:需標(biāo)注生產(chǎn)企業(yè)名稱(chēng)、生產(chǎn)日期、有效期、執(zhí)行標(biāo)準(zhǔn)號(hào)及“消字號(hào)”批準(zhǔn)文號(hào)(格式為省簡(jiǎn)稱(chēng)+衛(wèi)消證字+年份+編號(hào))。
3. 委托生產(chǎn)風(fēng)險(xiǎn):委托方需對(duì)產(chǎn)品質(zhì)量全程負(fù)責(zé),若受托方生產(chǎn)條件不達(dá)標(biāo),備案可能被撤銷(xiāo)。
通過(guò)系統(tǒng)化備案管理與嚴(yán)格自查,企業(yè)可有效規(guī)避違規(guī)風(fēng)險(xiǎn),確保產(chǎn)品合法上市。

站點(diǎn)聲明
本網(wǎng)站所提供的信息僅供參考之用,并不代表本網(wǎng)贊同其觀點(diǎn),也不代表本網(wǎng)對(duì)其真實(shí)性負(fù)責(zé)。圖片版權(quán)歸原作者所有,如有侵權(quán)請(qǐng)聯(lián)系我們,我們立刻刪除。如有關(guān)于作品內(nèi)容、版權(quán)或其它問(wèn)題請(qǐng)于作品發(fā)表后的30日內(nèi)與本站聯(lián)系,本網(wǎng)將迅速給您回應(yīng)并做相關(guān)處理。
鄭州思途醫(yī)療科技有限公司專(zhuān)注于醫(yī)療器械產(chǎn)品政策與法規(guī)規(guī)事務(wù)服務(wù),提供產(chǎn)品注冊(cè)備案申報(bào)代理、臨床試驗(yàn)、體系建立輔導(dǎo)、分類(lèi)界定、申請(qǐng)創(chuàng)新辦理服務(wù)。

2020年8月14日,化妝品備案網(wǎng)系統(tǒng)和檢測(cè)系統(tǒng)更新了!國(guó)家化妝品備案查詢(xún)需要移步到新網(wǎng)址了!

SSU是Study Start Up的縮寫(xiě),從最初的項(xiàng)目準(zhǔn)備,到啟動(dòng)訪視(Site Initiation Visit)之前所有的準(zhǔn)備工作,對(duì)整個(gè)臨床研究項(xiàng)目的啟動(dòng)非常關(guān)鍵。負(fù)責(zé)這個(gè)關(guān)鍵階段工作的部門(mén)人員,就叫做SS

初次申請(qǐng)消字號(hào)備案,總會(huì)遇到磕磕絆絆的問(wèn)題,常見(jiàn)的有申請(qǐng)流程、申請(qǐng)資料、申請(qǐng)周期等問(wèn)題,本文將對(duì)申請(qǐng)消字號(hào)產(chǎn)品流程及費(fèi)用簡(jiǎn)單概述,對(duì)即將進(jìn)入消毒產(chǎn)品行業(yè)的企業(yè)做一
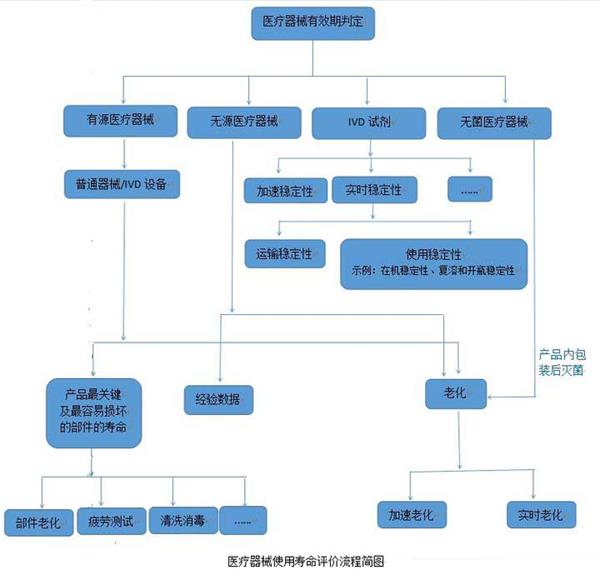
醫(yī)療器械的使用壽命是指醫(yī)療器械從規(guī)劃、設(shè)計(jì)、生產(chǎn)、銷(xiāo)售、安裝調(diào)試到使用、維修、維護(hù)檢測(cè)、報(bào)廢的全過(guò)程。而醫(yī)院使用的醫(yī)療器械的應(yīng)用質(zhì)量和安全管理在整個(gè)壽命過(guò)程中占重

在臨床試驗(yàn)中,無(wú)論是監(jiān)查員、質(zhì)控人員或者項(xiàng)目管理人員到研究中心查看項(xiàng)目資料的時(shí)候,總會(huì)多多少少發(fā)現(xiàn)一些問(wèn)題,有些問(wèn)題可能大家都比較熟知,但處理手法五花八門(mén)的。處理

脫落是每個(gè)臨床試驗(yàn)中都會(huì)出現(xiàn)并且也最讓人頭痛的現(xiàn)象。但是是什么原因引起脫落而我們?cè)趺床拍軠p少脫落呢?那么我們來(lái)談一下,項(xiàng)目中常見(jiàn)的脫落問(wèn)題,希望能為各位項(xiàng)目人員提

目前化妝品都要求必須進(jìn)行備案的,如果不備案就是違法的情況。所以必須進(jìn)行備案。已經(jīng)拿到資質(zhì)的化妝品備案編號(hào)在哪里找?怎么找?本文分享常見(jiàn)的化妝品備案編號(hào)查詢(xún)方法。
你是否遇到過(guò)這樣的問(wèn)題,國(guó)產(chǎn)化妝品小品牌不少,怕買(mǎi)到假冒偽劣產(chǎn)品,現(xiàn)在的仿造化妝品也不少,外包裝還同樣有防偽標(biāo)簽,就很頭疼。那么,查詢(xún)國(guó)產(chǎn)非特殊用途化妝品備案信息

我國(guó)GCP的附錄中也列出了類(lèi)似必備文件,詳細(xì)內(nèi)容讀者可以參考這兩個(gè)規(guī)范的附錄部分。——《藥物臨床試驗(yàn)與GCP實(shí)用指南》......下面介紹研究者應(yīng)當(dāng)保存的重要文件及要求。"

臨床試驗(yàn)從篩選到立項(xiàng)、啟動(dòng)、入組和中心關(guān)閉是一個(gè)完整的閉環(huán),什么時(shí)候可以開(kāi)始關(guān)閉中心?關(guān)閉中心需要做哪些事情?從哪里著手?今天我們就來(lái)談一談臨床試驗(yàn)關(guān)中心階段的那
行業(yè)資訊
?
?
?
?
?
?
知識(shí)分享
?
?
?
?
?
?
法規(guī)文件
?
?
?
?
?
?
八年
醫(yī)療器械服務(wù)經(jīng)驗(yàn)
聯(lián)系思途,免費(fèi)獲得專(zhuān)屬《落地解決方案》及報(bào)價(jià)
咨詢(xún)相關(guān)問(wèn)題或咨詢(xún)報(bào)價(jià),可以直接與我們聯(lián)系
思途CRO——醫(yī)療器械注冊(cè)臨床第三方平臺(tái)
