FDA指南|磁共振線圈產(chǎn)品性能接受標(biāo)準(zhǔn)
FDA于2020.12.11發(fā)布了關(guān)于簡(jiǎn)短(Abbreviated) 510(k)申請(qǐng)的相關(guān)產(chǎn)品指南,該指南是在遵守“基于安全有效性途徑”這一前提下編制提出的。在這個(gè)框架下,申請(qǐng)人若計(jì)劃使用安全有效性途徑提交


注冊(cè)備案 · 臨床試驗(yàn) · 體系建立輔導(dǎo) · 分類(lèi)界定 · 申請(qǐng)創(chuàng)新
來(lái)源:醫(yī)療器械注冊(cè)代辦 發(fā)布日期:2023-10-10 閱讀量:次
?

發(fā)布日期:2021-12-31 17:27
山東省藥品監(jiān)督管理局
關(guān)于印發(fā)《山東省醫(yī)療器械潔凈室(區(qū))現(xiàn)場(chǎng)檢查指南》等三項(xiàng)檢查指南的通知
魯藥監(jiān)械〔2021〕35號(hào)
省局有關(guān)處室、各檢查分局,有關(guān)直屬單位:
為進(jìn)一步規(guī)范醫(yī)療器械生產(chǎn)現(xiàn)場(chǎng)檢查工作,指導(dǎo)相關(guān)企業(yè)加強(qiáng)醫(yī)療器械生產(chǎn)質(zhì)量管理,省局組織編寫(xiě)了《山東省醫(yī)療器械潔凈室(區(qū))現(xiàn)場(chǎng)檢查指南》《山東省醫(yī)療器械工藝用水現(xiàn)場(chǎng)檢查指南》和《山東省手術(shù)無(wú)影燈生產(chǎn)現(xiàn)場(chǎng)檢查指南》,經(jīng)局務(wù)會(huì)審議通過(guò),現(xiàn)印發(fā)給你們,請(qǐng)結(jié)合實(shí)際參考執(zhí)行。
山東省藥品監(jiān)督管理局
2021年12月31日
(公開(kāi)屬性:主動(dòng)公開(kāi))
1.《山東省醫(yī)療器械潔凈室(區(qū))現(xiàn)場(chǎng)檢查指南》
2.《山東省醫(yī)療器械工藝用水現(xiàn)場(chǎng)檢查指南》
3.《山東省手術(shù)無(wú)影燈生產(chǎn)現(xiàn)場(chǎng)檢查指南》


站點(diǎn)聲明
本網(wǎng)站所提供的信息僅供參考之用,并不代表本網(wǎng)贊同其觀點(diǎn),也不代表本網(wǎng)對(duì)其真實(shí)性負(fù)責(zé)。圖片版權(quán)歸原作者所有,如有侵權(quán)請(qǐng)聯(lián)系我們,我們立刻刪除。如有關(guān)于作品內(nèi)容、版權(quán)或其它問(wèn)題請(qǐng)于作品發(fā)表后的30日內(nèi)與本站聯(lián)系,本網(wǎng)將迅速給您回應(yīng)并做相關(guān)處理。
鄭州思途醫(yī)療科技有限公司專(zhuān)注于醫(yī)療器械產(chǎn)品政策與法規(guī)規(guī)事務(wù)服務(wù),提供產(chǎn)品注冊(cè)備案申報(bào)代理、臨床試驗(yàn)、體系建立輔導(dǎo)、分類(lèi)界定、申請(qǐng)創(chuàng)新辦理服務(wù)。

FDA于2020.12.11發(fā)布了關(guān)于簡(jiǎn)短(Abbreviated) 510(k)申請(qǐng)的相關(guān)產(chǎn)品指南,該指南是在遵守“基于安全有效性途徑”這一前提下編制提出的。在這個(gè)框架下,申請(qǐng)人若計(jì)劃使用安全有效性途徑提交

為規(guī)范醫(yī)療器械(含體外診斷試劑)注冊(cè)管理,根據(jù)國(guó)家藥監(jiān)局《關(guān)于公布醫(yī)療器械注冊(cè)申報(bào)資料要求和批準(zhǔn)證明文件格式的公告》(2021年第121號(hào))、《關(guān)于公布體外診斷試劑注冊(cè)申報(bào)

為規(guī)范醫(yī)療器械(含體外診斷試劑)注冊(cè)管理,根據(jù)國(guó)家藥監(jiān)局《關(guān)于公布醫(yī)療器械注冊(cè)申報(bào)資料要求和批準(zhǔn)證明文件格式的公告》(2021年第121號(hào))、《關(guān)于公布體外診斷試劑注冊(cè)申報(bào)

思途給大家提供近日,《2021年長(zhǎng)三角醫(yī)保一體化工作要點(diǎn)?》在業(yè)內(nèi)流傳,文件顯示,上海、江蘇、浙江、安徽三省一市醫(yī)保局將在長(zhǎng)三角實(shí)行統(tǒng)一的醫(yī)保目錄,加強(qiáng)長(zhǎng)三角藥品耗材招采
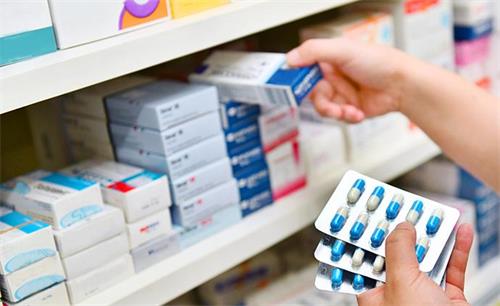
藥品零售企業(yè)是否實(shí)施GSP認(rèn)證,被國(guó)際社會(huì)看成藥品經(jīng)營(yíng)質(zhì)量有無(wú)保證的先決條件。能否正確把握《藥品零售企業(yè)GSP認(rèn)證檢查評(píng)定標(biāo)準(zhǔn)》和《藥品零售企業(yè)GSP認(rèn)證現(xiàn)場(chǎng)檢查項(xiàng)目》精"

為規(guī)范醫(yī)療器械(含體外診斷試劑)注冊(cè)管理,根據(jù)國(guó)家藥監(jiān)局《關(guān)于公布醫(yī)療器械注冊(cè)申報(bào)資料要求和批準(zhǔn)證明文件格式的公告》(2021年第121號(hào))、《關(guān)于公布體外診斷試劑注冊(cè)申報(bào)
為落實(shí)《醫(yī)療器械監(jiān)督管理?xiàng)l例》(國(guó)務(wù)院令第739號(hào))要求,根據(jù)《醫(yī)療器械注冊(cè)與備案管理辦法》(市場(chǎng)監(jiān)管總局令第47號(hào))《體外診斷試劑注冊(cè)與備案管理辦法》(市場(chǎng)監(jiān)管總局令第48號(hào)),

為加強(qiáng)醫(yī)療器械產(chǎn)品注冊(cè)工作的監(jiān)督和指導(dǎo),進(jìn)一步提高注冊(cè)審查質(zhì)量,國(guó)家藥品監(jiān)督管理局組織制定了《關(guān)節(jié)鏡下無(wú)源手術(shù)器械產(chǎn)品注冊(cè)審查指導(dǎo)原則》《一次性使用輸尿管導(dǎo)引鞘注
為落實(shí)《醫(yī)療器械監(jiān)督管理?xiàng)l例》(國(guó)務(wù)院令第739號(hào))要求,根據(jù)《醫(yī)療器械注冊(cè)與備案管理辦法》(市場(chǎng)監(jiān)管總局令第47號(hào))和《體外診斷試劑注冊(cè)與備案管理辦法》(市場(chǎng)監(jiān)管總局令第48號(hào)

申辦方/CRO有意向在我院開(kāi)展臨床試驗(yàn)項(xiàng)目時(shí),需要提交相關(guān)材料與臨床研究管理部進(jìn)行意向溝通。遞交材料包括臨床試驗(yàn)意向溝通信息登記表(附件)、NMPA臨床試驗(yàn)批件/溝通函、方案摘要
行業(yè)資訊
?
?
?
?
?
?
知識(shí)分享
法規(guī)文件
?
?
?
?
?
?
八年
醫(yī)療器械服務(wù)經(jīng)驗(yàn)
聯(lián)系思途,免費(fèi)獲得專(zhuān)屬《落地解決方案》及報(bào)價(jià)
咨詢(xún)相關(guān)問(wèn)題或咨詢(xún)報(bào)價(jià),可以直接與我們聯(lián)系
思途CRO——醫(yī)療器械注冊(cè)臨床第三方平臺(tái)
