【國家化妝品備案查詢】國家化妝品備案查詢網(wǎng)站入口
2020年8月14日,化妝品備案網(wǎng)系統(tǒng)和檢測系統(tǒng)更新了!國家化妝品備案查詢需要移步到新網(wǎng)址了!


注冊備案 · 臨床試驗 · 體系建立輔導 · 分類界定 · 申請創(chuàng)新
來源:醫(yī)療器械注冊代辦 發(fā)布日期:2024-01-08 閱讀量:次
目前國內(nèi)建設了“”藥物臨床試驗與信息公示平臺”,所有在中國境內(nèi)進行的由藥廠作為申辦者或者提供資金的臨床試驗均可查詢。但是在如何查詢已經(jīng)開展的醫(yī)療器械臨床試驗呢?

目前并不能完全進行查詢,只有在平臺已經(jīng)注冊的醫(yī)療器械臨床試驗才可以查詢,國際醫(yī)學雜志編輯委員會(InternationalCommittee of Medical Journal Editors,ICMJE)宣布,從2005年7月1日起不出版未注冊的臨床試驗論文。對于研究者發(fā)起的研究,很多都可以查詢到,而對于大量申辦方開展的以上市為目的的臨床試驗并不需要在國際發(fā)表,能查詢到的較少。
目前小編經(jīng)常用的主要是以下兩個網(wǎng)站進行查詢,收獲還是蠻大的,特此向大家推薦下:
1、中國臨床試驗注冊中心:https://www.chictr.org.cn/searchproj.html
該網(wǎng)站是WHO臨床試驗和國際醫(yī)學期刊編輯委員會(>ICMJE)注冊的中國平臺,該平臺除包含藥物臨床試驗試驗外,還可以查詢到已經(jīng)注冊的醫(yī)療器械臨床試驗。中國臨床試驗注冊中心由衛(wèi)生部中國循證醫(yī)學中心和四川大學華西醫(yī)院等共同組建。臨床試驗注冊不僅能確保追溯每個臨床試驗的結果,而且公開在研試驗或?qū)嶒灲Y果信息還有助于減少不必要的重復研究。是繼澳大利亞臨床試驗注冊中心等之后的世界第四個一級注冊機構。需要在受試者入組前提交注冊,如果補注冊,還要交3000元人民幣。
2、FDA臨床試驗公示平臺:https://clinicaltrials.gov/
該網(wǎng)站是FDA的臨床試驗公示系統(tǒng),不僅可以查詢到美國的臨床試驗,還可以按疾病、國家和地區(qū)進行檢索,可以查到大量的中國試驗。包括很多的醫(yī)療器械臨床試驗。
這兩個網(wǎng)站是小編用的最多的,可以查詢到入排標準,主要指標和次要指標,觀察周期等,基本也是臨床試驗方案的核心內(nèi)容,對小編進行同類醫(yī)療器械產(chǎn)品方案的撰寫起到了很大的幫助作用。
3、如果以上兩個網(wǎng)站查詢不到,大家還可以登錄世界衛(wèi)生組織,歐盟,澳大利亞、印度等超多的數(shù)據(jù)庫進行查詢,如下:
| Australian New Zealand Clinical Trials Registry (ANZCTR) |
| Brazilian Clinical Trials Registry (ReBec) |
| Chinese Clinical Trial Registry (ChiCTR) |
| Clinical Research Information Service (CRiS), Republic of Korea |
| Clinical Trials Registry - India (CTRI) |
| Cuban Public Registry of Clinical Trials(RPCEC) |
| EU Clinical Trials Register (EU-CTR) |
| German Clinical Trials Register (DRKS) |
| Iranian Registry of Clinical Trials (IRCT) |
| ISRCTN |
| Japan Primary Registries Network (JPRN) |
| Thai Clinical Trials Registry (TCTR) |
| The Netherlands National Trial Register (NTR) |
| Pan African Clinical Trial Registry (PACTR) |
| Peruvian Clinical Trial Registry (REPEC) |
| Sri Lanka Clinical Trials Registry (SLCTR) |
作者:Stone

站點聲明
本網(wǎng)站所提供的信息僅供參考之用,并不代表本網(wǎng)贊同其觀點,也不代表本網(wǎng)對其真實性負責。圖片版權歸原作者所有,如有侵權請聯(lián)系我們,我們立刻刪除。如有關于作品內(nèi)容、版權或其它問題請于作品發(fā)表后的30日內(nèi)與本站聯(lián)系,本網(wǎng)將迅速給您回應并做相關處理。
鄭州思途醫(yī)療科技有限公司專注于醫(yī)療器械產(chǎn)品政策與法規(guī)規(guī)事務服務,提供產(chǎn)品注冊備案申報代理、臨床試驗、體系建立輔導、分類界定、申請創(chuàng)新辦理服務。

2020年8月14日,化妝品備案網(wǎng)系統(tǒng)和檢測系統(tǒng)更新了!國家化妝品備案查詢需要移步到新網(wǎng)址了!

盲法試驗常用的有兩種:單盲(single blinding)和雙盲(double blinding),更嚴格的對照試驗要用到三盲(triple blinding),在對照藥物和試驗藥物劑型或外觀不同時,還要用到雙盲雙模擬技

剛接觸CRO行業(yè)的小伙伴,在學習文件法規(guī)資料的同時,常看到一些英文類專業(yè)名詞不知道是什么意思。下面,一起看看常見的臨床試驗專業(yè)術語: CRO行業(yè)的常用術語解釋: 1:新藥研發(fā)

SSU是Study Start Up的縮寫,從最初的項目準備,到啟動訪視(Site Initiation Visit)之前所有的準備工作,對整個臨床研究項目的啟動非常關鍵。負責這個關鍵階段工作的部門人員,就叫做SS
試驗用藥品是指用于臨床試驗的試驗藥物、對照藥品。試驗用藥品滲透到了臨床試驗過程中的每一個步驟,包括藥物的生產(chǎn)、包裝、運輸、保存、使用、回收等。今天我們從臨床試驗中

從事醫(yī)療器械注冊的小伙伴們可能都為同一個問題苦惱過,那就是醫(yī)療器械注冊單元的劃分。企業(yè)所設計開發(fā)出的產(chǎn)品,其所包含的產(chǎn)品范圍,是否可通過一個注冊單元完成注冊,從而

不少二三類需要臨床的產(chǎn)品,客戶一聽到臨床報價就退縮。既然這么貴,還不如自己做......事實真的是這樣嗎?臨床報價費用都由哪些組成?費用都誰收走了?自己做又有哪些風險?文

醫(yī)學的進步是以研究為基礎的,這些研究在一定程度上賴于以人作為受試者的試驗。--《赫爾辛基宣言》。Ⅰ期臨床研究目的是確定可用于臨床新藥的安全有效劑量與合理給藥方案。根據(jù)
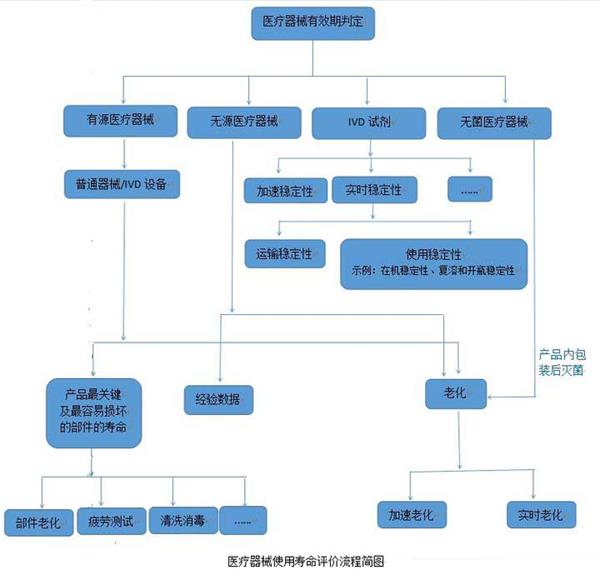
醫(yī)療器械的使用壽命是指醫(yī)療器械從規(guī)劃、設計、生產(chǎn)、銷售、安裝調(diào)試到使用、維修、維護檢測、報廢的全過程。而醫(yī)院使用的醫(yī)療器械的應用質(zhì)量和安全管理在整個壽命過程中占重

俗話說“知己知彼,百戰(zhàn)不殆”,對于作為CRC的我們,自認為對CRA其實已經(jīng)很了解了,但是在我們工作過程有一個角色平時接觸不到,但是卻又繞不開躲不過,尤其是面對滿屏EDC query的
行業(yè)資訊
?
?
?
?
?
?
知識分享
八年
醫(yī)療器械服務經(jīng)驗
聯(lián)系思途,免費獲得專屬《落地解決方案》及報價
咨詢相關問題或咨詢報價,可以直接與我們聯(lián)系
思途CRO——醫(yī)療器械注冊臨床第三方平臺
