臨床脫落是什么意思?脫落原因有哪些?如何降低脫落率?
脫落是每個(gè)臨床試驗(yàn)中都會(huì)出現(xiàn)并且也最讓人頭痛的現(xiàn)象。但是是什么原因引起脫落而我們?cè)趺床拍軠p少脫落呢?那么我們來(lái)談一下,項(xiàng)目中常見(jiàn)的脫落問(wèn)題,希望能為各位項(xiàng)目人員提


注冊(cè)備案 · 臨床試驗(yàn) · 體系建立輔導(dǎo) · 分類界定 · 申請(qǐng)創(chuàng)新
來(lái)源:醫(yī)療器械注冊(cè)代辦 發(fā)布日期:2025-08-25 閱讀量:次
在醫(yī)療器械或藥物臨床試驗(yàn)中,“受試者知情同意”是核心環(huán)節(jié)。它不僅是法規(guī)要求的必須步驟,更是保護(hù)受試者權(quán)益的基石。很多初次接觸研究的人,包括部分基層研究人員,可能會(huì)把“知情同意”這個(gè)過(guò)程和最后簽字的“知情同意書”文件混為一談。其實(shí)這是兩件緊密相關(guān)但完全不同的事。搞清楚它們的區(qū)別,弄明白如何規(guī)范操作,是開(kāi)展合規(guī)臨床研究的第一步。

“知情同意”是一個(gè)完整的、動(dòng)態(tài)的溝通過(guò)程。它指的是研究者用受試者能完全聽(tīng)懂的大白話,把試驗(yàn)的所有關(guān)鍵信息都解釋清楚。這些信息包括試驗(yàn)?zāi)康摹⒘鞒獭⒊掷m(xù)時(shí)間、預(yù)期的風(fēng)險(xiǎn)和潛在獲益、其他可選擇的治療方案,以及受試者的權(quán)利(比如隨時(shí)可以無(wú)條件退出)。核心在于確保受試者在充分理解的基礎(chǔ)上,自愿做出是否參加的決定。這個(gè)過(guò)程強(qiáng)調(diào)的是一種“有效的溝通”,而不是簡(jiǎn)單的“念文件”和“簽字”。
“知情同意書”則是上面那個(gè)溝通過(guò)程完成后的書面證明文件。它把口頭溝通的所有關(guān)鍵信息用文字形式固定下來(lái),最后由受試者(或其監(jiān)護(hù)人)簽名并注明日期,作為同意參加的法律憑證。這份文件是備案用的,是過(guò)程的結(jié)果。可以說(shuō),“知情同意”是過(guò)程和行動(dòng),“知情同意書”是記錄這個(gè)行動(dòng)結(jié)果的文件和證據(jù)。
| 對(duì)比維度 | 知情同意 (過(guò)程) | 知情同意書 (文件) |
|---|---|---|
| 性質(zhì) | 一個(gè)持續(xù)的、雙向的溝通和教育過(guò)程 | 一份靜態(tài)的、記錄溝通結(jié)果的書面法律文件 |
| 核心 | 確保“充分理解”和“自愿同意” | 提供“書面證據(jù)”和“簽名備案” |
| 形式 | 研究者與受試者之間的對(duì)話、問(wèn)答、交流 | 一份由受試者簽署并注明日期的紙質(zhì)文檔 |
| 關(guān)系 | 先有完整、合規(guī)的“知情同意”過(guò)程,才會(huì)有有效簽署的“知情同意書”文件。文件是過(guò)程的證明。 | |
獲得知情同意書有嚴(yán)格的步驟,不是簡(jiǎn)單地把文件遞給受試者簽字。首先,必須由主要研究者或其授權(quán)的、經(jīng)過(guò)培訓(xùn)的團(tuán)隊(duì)成員來(lái)執(zhí)行這個(gè)過(guò)程。其次,要在受試者參加任何試驗(yàn)相關(guān)檢查之前進(jìn)行,確保決定是在沒(méi)有任何干預(yù)的情況下做出的。談話時(shí)要給予受試者及其家人充足的時(shí)間提問(wèn)和考慮,不能催促。最后,在受試者確認(rèn)對(duì)所有內(nèi)容無(wú)疑問(wèn)并完全理解后,方可簽署知情同意書。簽署后,受試者應(yīng)保留一份副本以備查閱。對(duì)于兒童、意識(shí)不清等無(wú)法自己同意的受試者,必須由其法定代理人代為同意,整個(gè)過(guò)程還需要有中立的見(jiàn)證人在場(chǎng)監(jiān)督并簽字。
總結(jié)來(lái)說(shuō),知情同意是一個(gè)重在溝通和理解的過(guò)程,而知情同意書是這個(gè)過(guò)程的書面記錄和證明。前者是后者的基礎(chǔ)和前提,后者是前者的結(jié)果和形式。規(guī)范地完成整個(gè)過(guò)程并獲得簽署的文件,是尊重受試者自主權(quán)、保障其合法權(quán)益的核心操作,必須嚴(yán)格按照國(guó)家《藥物臨床試驗(yàn)質(zhì)量管理規(guī)范》的要求來(lái)執(zhí)行,容不得半點(diǎn)馬虎。

站點(diǎn)聲明
本網(wǎng)站所提供的信息僅供參考之用,并不代表本網(wǎng)贊同其觀點(diǎn),也不代表本網(wǎng)對(duì)其真實(shí)性負(fù)責(zé)。圖片版權(quán)歸原作者所有,如有侵權(quán)請(qǐng)聯(lián)系我們,我們立刻刪除。如有關(guān)于作品內(nèi)容、版權(quán)或其它問(wèn)題請(qǐng)于作品發(fā)表后的30日內(nèi)與本站聯(lián)系,本網(wǎng)將迅速給您回應(yīng)并做相關(guān)處理。
鄭州思途醫(yī)療科技有限公司專注于醫(yī)療器械產(chǎn)品政策與法規(guī)規(guī)事務(wù)服務(wù),提供產(chǎn)品注冊(cè)備案申報(bào)代理、臨床試驗(yàn)、體系建立輔導(dǎo)、分類界定、申請(qǐng)創(chuàng)新辦理服務(wù)。

脫落是每個(gè)臨床試驗(yàn)中都會(huì)出現(xiàn)并且也最讓人頭痛的現(xiàn)象。但是是什么原因引起脫落而我們?cè)趺床拍軠p少脫落呢?那么我們來(lái)談一下,項(xiàng)目中常見(jiàn)的脫落問(wèn)題,希望能為各位項(xiàng)目人員提
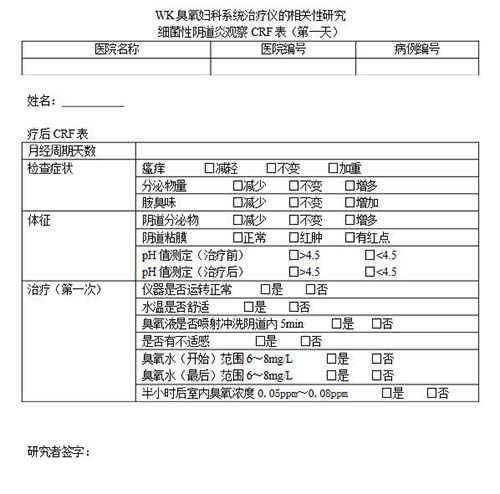
病例報(bào)告表(case report form,CRF)是按照臨床試驗(yàn)方案的要求設(shè)計(jì)的書面文件,用于記錄和報(bào)告每一名受試者在試驗(yàn)過(guò)程中的數(shù)據(jù),這種文件一般采用表格(紙質(zhì)或電子)的形式。"

隨著越來(lái)越多的臨床試驗(yàn)中都配備 CRA,CRA 與 CRC 在臨床試驗(yàn)中的作用及合作值得大家一起探討。首先,介紹一下在項(xiàng)目運(yùn)行中可能出現(xiàn)的問(wèn)題和矛盾,間接影響了項(xiàng)目的執(zhí)行和質(zhì)量。希

作為一名苦逼的CRA,除了日常的監(jiān)查工作以外,也許還有一個(gè)讓人很頭疼的問(wèn)題,每次項(xiàng)目會(huì)議上PM重復(fù)又重復(fù)了的話題:“親,這個(gè)Site的進(jìn)度太慢啦,想想辦法啊!CRA:我在想 我在想

臨床CCG是什么意思?CCG是數(shù)據(jù)填寫指南,由DM起草,相關(guān)人員審核,可能包括PM,醫(yī)學(xué),藥物警戒等,主要是給數(shù)據(jù)庫(kù)錄入人員CRC.PI.以及發(fā)布質(zhì)疑的CRA和醫(yī)學(xué)使用的指南文件。

在臨床試驗(yàn)方案的設(shè)計(jì)過(guò)程中,大家都會(huì)盡可能的考慮到各種可能影響試驗(yàn)的因素,并制定標(biāo)準(zhǔn)操作規(guī)程,盡量避免和減少在試驗(yàn)中可能出現(xiàn)違背及偏離方案的情況發(fā)生,但在試驗(yàn)的執(zhí)

通過(guò)電話或面對(duì)面進(jìn)行潛在受試者的預(yù)篩選,以確定受試者最初的合格性和其對(duì)研究的興趣是招募過(guò)程中常見(jiàn)的策略。需要注意的是在使用此策略時(shí),研究者必須保護(hù)潛在受試者的隱私

大家在項(xiàng)目中,是否遇到過(guò)ICF更新的情況?在ICF更新后,已由受試者簽署的知情同意書,是否需要重新簽署呢?又有哪些情形不需要重新簽署呢?本期我們繼續(xù)跟大家分享知情同意書實(shí)

NCCN(美國(guó)國(guó)立綜合癌癥網(wǎng)絡(luò))指南是目前國(guó)際上最權(quán)威、最廣泛采用的癌癥治療指南。NCCN指南明確指出: 治療選擇之一就是參加臨床試驗(yàn) 。 在歐美國(guó)家很多患者會(huì)主動(dòng)咨詢醫(yī)生是否

招募廣告是臨床試驗(yàn)中用以招募受試者的一種方法,隨著藥物、器械臨床試驗(yàn)以及研究者發(fā)起的涉及人的生物醫(yī)學(xué)研究越來(lái)越廣泛地開(kāi)展,臨床試驗(yàn)中招募廣告的使用也日益頻繁,甚至
行業(yè)資訊
?
?
?
?
?
?
知識(shí)分享
法規(guī)文件
?
?
?
?
?
?
八年
醫(yī)療器械服務(wù)經(jīng)驗(yàn)
聯(lián)系思途,免費(fèi)獲得專屬《落地解決方案》及報(bào)價(jià)
咨詢相關(guān)問(wèn)題或咨詢報(bào)價(jià),可以直接與我們聯(lián)系
思途CRO——醫(yī)療器械注冊(cè)臨床第三方平臺(tái)
