干貨|臨床SSU工作內(nèi)容和具體工作流程
SSU是Study Start Up的縮寫,從最初的項(xiàng)目準(zhǔn)備,到啟動(dòng)訪視(Site Initiation Visit)之前所有的準(zhǔn)備工作,對(duì)整個(gè)臨床研究項(xiàng)目的啟動(dòng)非常關(guān)鍵。負(fù)責(zé)這個(gè)關(guān)鍵階段工作的部門人員,就叫做SS


注冊(cè)備案 · 臨床試驗(yàn) · 體系建立輔導(dǎo) · 分類界定 · 申請(qǐng)創(chuàng)新
來源:醫(yī)療器械注冊(cè)代辦 發(fā)布日期:2023-10-10 閱讀量:次
?
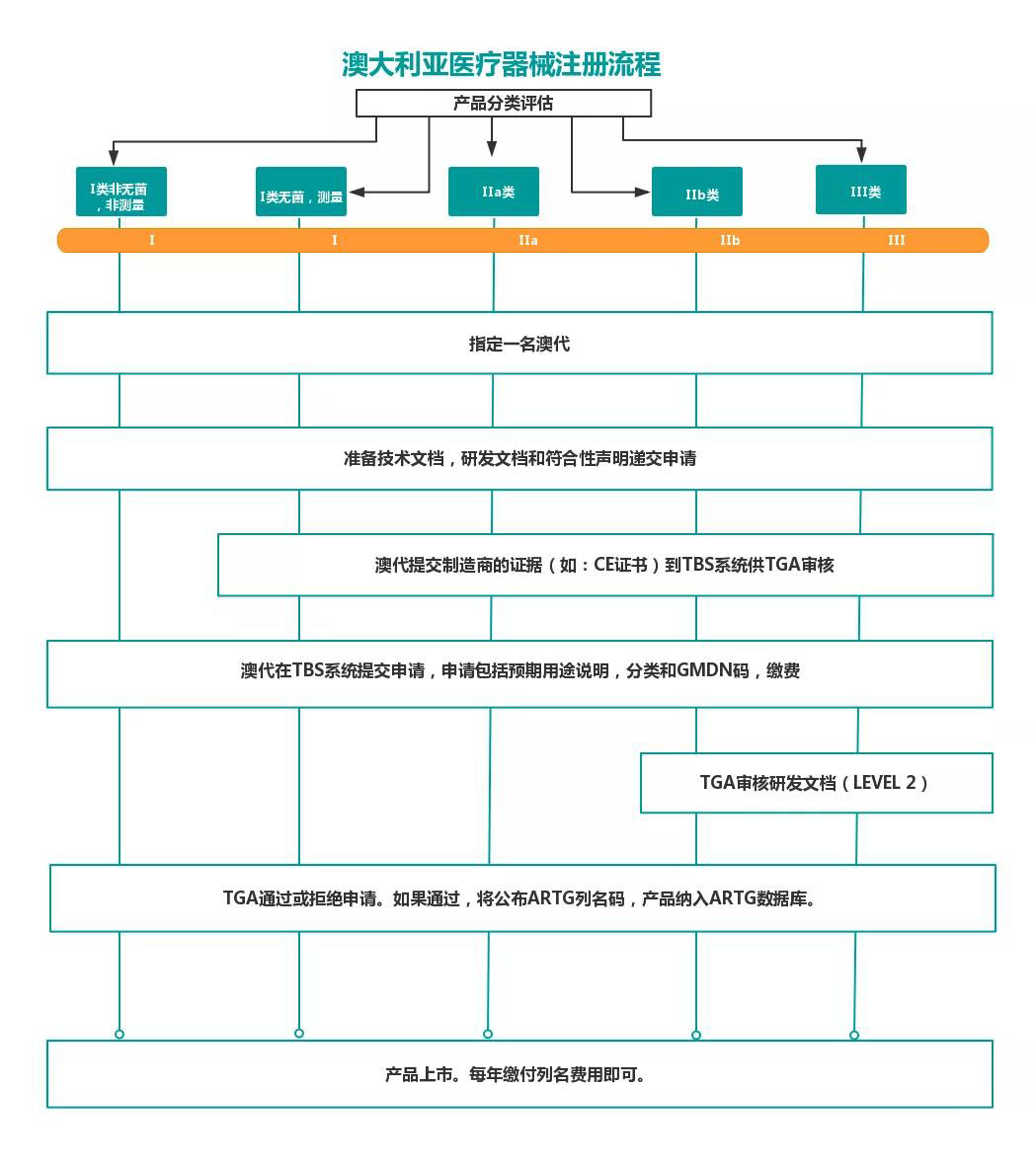
引言:任何國家醫(yī)療器械產(chǎn)品出口澳大利亞,需經(jīng)歷TGA注冊(cè),以下是關(guān)于澳大利亞醫(yī)療器械注冊(cè)知識(shí)點(diǎn),簡(jiǎn)單了解一下,文中大致概括了注冊(cè)全流程,未標(biāo)明細(xì)節(jié),如有產(chǎn)品需要澳大利亞注冊(cè)認(rèn)證,歡迎聯(lián)系在線客服。

澳大利亞TGA全稱是The Therapeutic Goods Administration,是澳大利亞政府衛(wèi)生部的一部分,負(fù)責(zé)管理治療用品,包括處方藥、疫苗、防曬霜、維生素和礦物質(zhì)、醫(yī)療設(shè)備、血液和血液制品。幾乎任何聲稱具有治療功效的產(chǎn)品都必須被登記在澳大利亞ARTG,然后才能在澳大利亞供應(yīng)。
The Therapeutic Goods Administration (TGA) is part of the Australian Government Department of Health, and is responsible for regulating therapeutic goods including prescription medicines, vaccines, sunscreens, vitamins and minerals, medical devices, blood and blood products. Almost any product for which therapeutic claims are made must be entered in the Australian Register of Therapeutic Goods (ARTG) before it can be supplied in Australia.
生產(chǎn)商需要提供如下資料以確定醫(yī)療器械分類:
The manufacturer is responsible for determining the classification of a device using a set of classification rules based on the:
1.醫(yī)療器械的預(yù)期用途。
·manufacturer’s intended use of the device
2.對(duì)病人,用戶及其他人的風(fēng)險(xiǎn)等級(jí)。
·level of risk to patients, users and other persons (the probability of occurrence of harm and the severity of that harm)
3.植入人體的程度。
·degree of invasiveness in the human body
4.使用時(shí)限。
·duration of use
其分類等級(jí)劃分如下表:
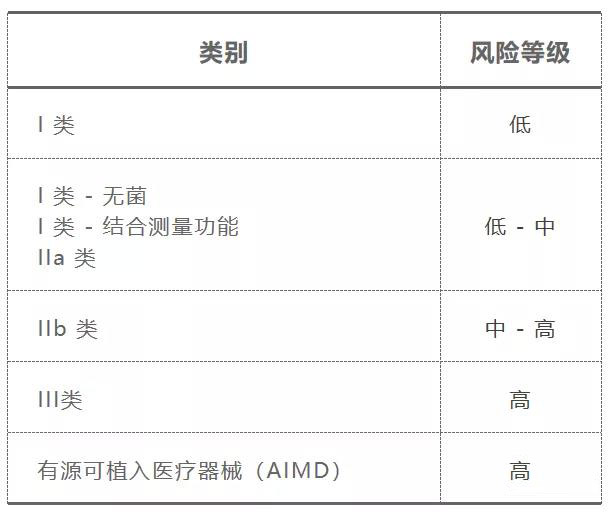
制造商必須能夠證明該器械以及制造該器械的過程符合澳大利亞相關(guān)法規(guī)的要求。
相關(guān)法規(guī)如下:
1.Therapeutic Goods Act 1989 (the Act)
2.Therapeutic Goods (Medical Devices) Regulations 2002 (the Regulations)
符合性評(píng)估證據(jù)類型:
The TGA accepts the following certificates as conformity assessment evidence:
1.TGA頒發(fā)的符合性評(píng)估證書(對(duì)部分企業(yè)是唯一途徑)
a TGA Conformity Assessment Certificate issued by the TGA - this is mandatory for some manufacturers
2.澳大利亞EC MRA 符合性證書
certificates of conformity issued under the Australia -EC MRA
3.澳大利亞 EFTA MRA 符合性證書
certificates of conformity issued under the Australia -EFTA MRA
4.由歐盟公告機(jī)構(gòu)頒發(fā)的EC證書
EC certificates issued by an EU Notified Body

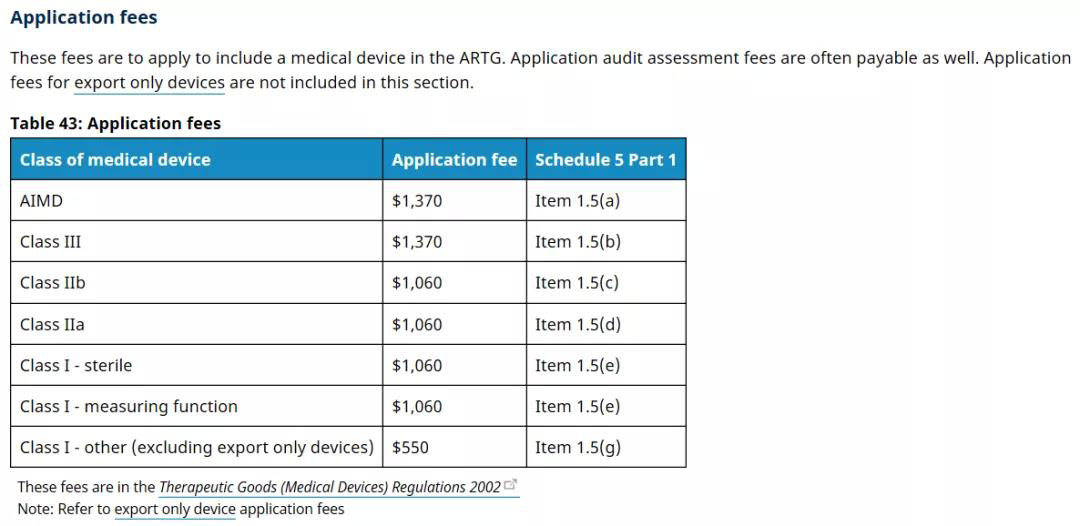
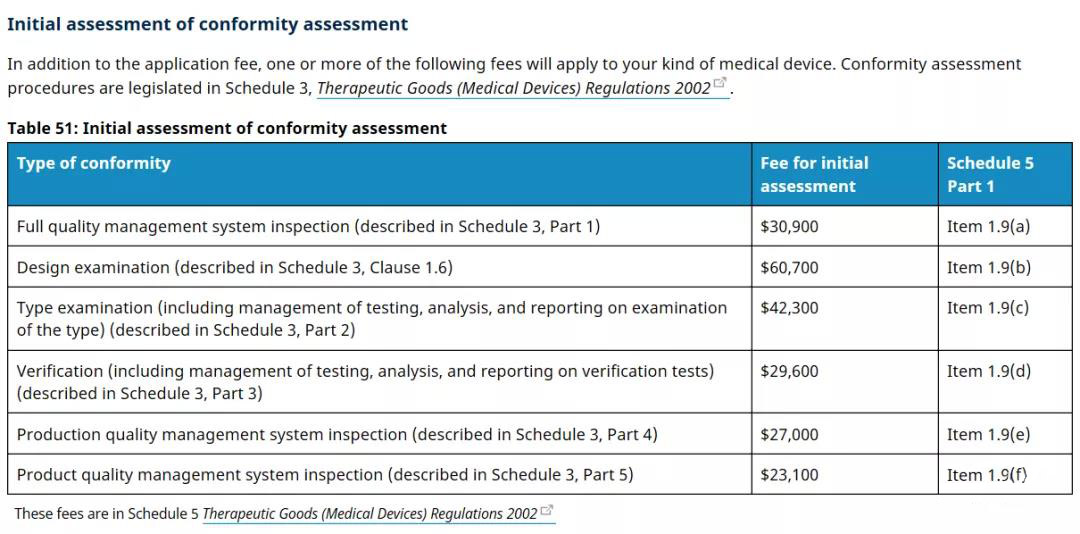

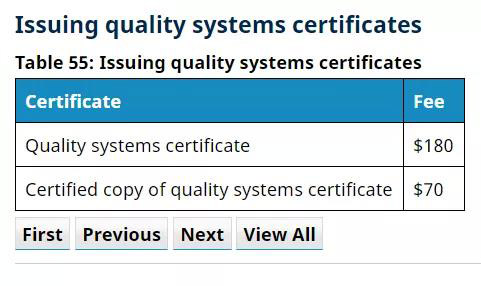
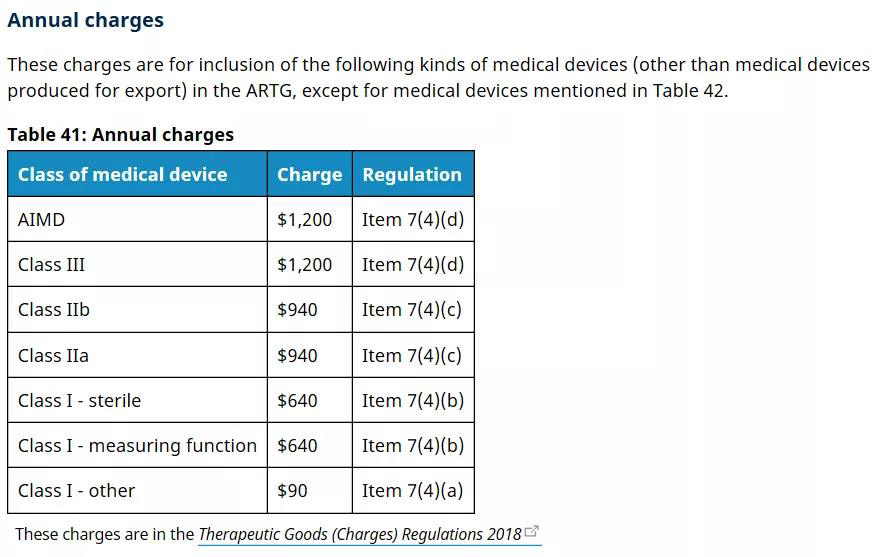
*由官方費(fèi)用具有可變動(dòng)性,實(shí)際費(fèi)用以實(shí)時(shí)價(jià)格為準(zhǔn)。

站點(diǎn)聲明
本網(wǎng)站所提供的信息僅供參考之用,并不代表本網(wǎng)贊同其觀點(diǎn),也不代表本網(wǎng)對(duì)其真實(shí)性負(fù)責(zé)。圖片版權(quán)歸原作者所有,如有侵權(quán)請(qǐng)聯(lián)系我們,我們立刻刪除。如有關(guān)于作品內(nèi)容、版權(quán)或其它問題請(qǐng)于作品發(fā)表后的30日內(nèi)與本站聯(lián)系,本網(wǎng)將迅速給您回應(yīng)并做相關(guān)處理。
鄭州思途醫(yī)療科技有限公司專注于醫(yī)療器械產(chǎn)品政策與法規(guī)規(guī)事務(wù)服務(wù),提供產(chǎn)品注冊(cè)備案申報(bào)代理、臨床試驗(yàn)、體系建立輔導(dǎo)、分類界定、申請(qǐng)創(chuàng)新辦理服務(wù)。

SSU是Study Start Up的縮寫,從最初的項(xiàng)目準(zhǔn)備,到啟動(dòng)訪視(Site Initiation Visit)之前所有的準(zhǔn)備工作,對(duì)整個(gè)臨床研究項(xiàng)目的啟動(dòng)非常關(guān)鍵。負(fù)責(zé)這個(gè)關(guān)鍵階段工作的部門人員,就叫做SS

初次申請(qǐng)消字號(hào)備案,總會(huì)遇到磕磕絆絆的問題,常見的有申請(qǐng)流程、申請(qǐng)資料、申請(qǐng)周期等問題,本文將對(duì)申請(qǐng)消字號(hào)產(chǎn)品流程及費(fèi)用簡(jiǎn)單概述,對(duì)即將進(jìn)入消毒產(chǎn)品行業(yè)的企業(yè)做一

從事醫(yī)療器械注冊(cè)的小伙伴們可能都為同一個(gè)問題苦惱過,那就是醫(yī)療器械注冊(cè)單元的劃分。企業(yè)所設(shè)計(jì)開發(fā)出的產(chǎn)品,其所包含的產(chǎn)品范圍,是否可通過一個(gè)注冊(cè)單元完成注冊(cè),從而
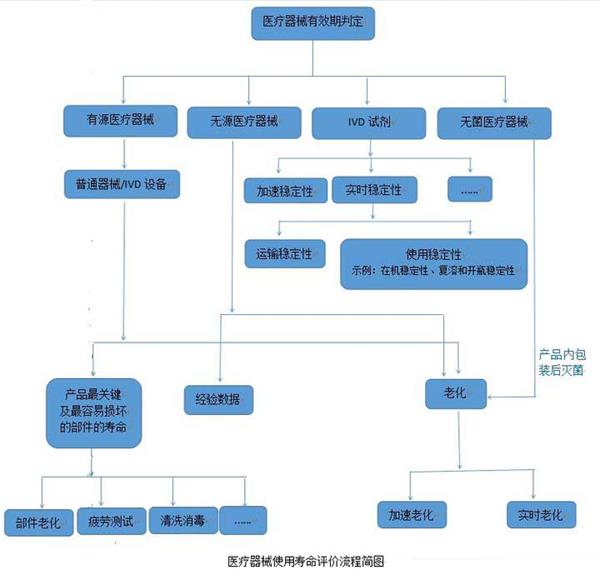
醫(yī)療器械的使用壽命是指醫(yī)療器械從規(guī)劃、設(shè)計(jì)、生產(chǎn)、銷售、安裝調(diào)試到使用、維修、維護(hù)檢測(cè)、報(bào)廢的全過程。而醫(yī)院使用的醫(yī)療器械的應(yīng)用質(zhì)量和安全管理在整個(gè)壽命過程中占重

大多數(shù)CRO公司在臨床試驗(yàn)現(xiàn)場(chǎng)啟動(dòng)會(huì)(SIV)上,常由CRA主導(dǎo)。作為一名有上進(jìn)心的CRA必須清楚的了解到臨床試驗(yàn)現(xiàn)場(chǎng)啟動(dòng)考察的流程,再分享一些本人在啟動(dòng)會(huì)考察的細(xì)節(jié),請(qǐng)看下文。

隨著醫(yī)療器械出口的日益增長,根據(jù)市場(chǎng)的需求各醫(yī)療器械生產(chǎn)廠商需要符合國家和地區(qū)的質(zhì)量體系法規(guī)越來越多,所以經(jīng)常會(huì)碰到出處于不同法規(guī)或標(biāo)準(zhǔn)的一些比較容易混淆的概念及

關(guān)中心訪視(Close Out Visits,簡(jiǎn)稱COV),想必大家都聽說過。作為臨床試驗(yàn)最后一個(gè)階段,COV也是非常重要的一個(gè)環(huán)節(jié),今天和大家分享一下作為監(jiān)查員在COV時(shí)應(yīng)該做哪些工作。什么時(shí)候

剛接觸醫(yī)療器械CRO行業(yè)的小伙伴,在學(xué)習(xí)文件法規(guī)資料的同時(shí),常看到一些英文類專業(yè)名詞不知道是什么意思。下面,一起看看常見的醫(yī)療器械臨床試驗(yàn)專業(yè)術(shù)語......"

2019年5月31日,國家藥監(jiān)局發(fā)布了《關(guān)于實(shí)施醫(yī)療器械注冊(cè)電子申報(bào)的公告(2019年第46號(hào))》,從2019年6月24日正式實(shí)施電子申報(bào),從11月1日起提交國家局的注冊(cè)資料都需要按照電子申報(bào)目錄

醫(yī)療器械注冊(cè)證是依照法定程序,對(duì)擬上市銷售、使用的醫(yī)療器械的安全性、有效性進(jìn)行評(píng)價(jià),決定同意其銷售、使用后發(fā)放的證件,由國家食品藥品監(jiān)督管理總局統(tǒng)一制定。"
行業(yè)資訊
知識(shí)分享
法規(guī)文件
?
?
?
?
?
?
八年
醫(yī)療器械服務(wù)經(jīng)驗(yàn)
聯(lián)系思途,免費(fèi)獲得專屬《落地解決方案》及報(bào)價(jià)
咨詢相關(guān)問題或咨詢報(bào)價(jià),可以直接與我們聯(lián)系
思途CRO——醫(yī)療器械注冊(cè)臨床第三方平臺(tái)
